La temporada gripal discurre entre la semana 40 de cada año y la semana 20 del año siguiente. Hasta la fecha el Ministerio de Sanidad no ha publicado los datos de coberturas vacunales correspondientes al año 2019, por lo que no está disponible la información en detalle de la cobertura de vacunación antigripal por comunidades autónomas.
El Centro Nacional de Epidemiología (CNE) ha publicado los datos de la vigilancia epidemiológica de la temporada gripal 2019-2020 en un informe en formato PDF de 35 páginas. Además, está disponible una infografía con un resumen del impacto de la gripe (ver imagen adjunta).
La temporada gripal 2019-2020 en España
El umbral epidémico (52,6 casos/100.000 habitantes) se superó por primera vez en la semana 1/2020, la incidencia máxima se alcanzó en la semana 5/2020 (270,3 casos/100.000) y la incidencia volvió a situarse por debajo del umbral en la semana 10/2020 (ver imagen adjunta, Sistema de vigilancia de la gripe en España). Datos similares a los de la temporada previa, 2018-2019.
Las fuentes de información proceden de 16 comunidades/ciudades autónomas (no están incluidas en la red de vigilancia epidemiológica de la gripe Aragón, Galicia y Murcia); participan en la red de médicos centinelas de atención primaria 555 médicos de familia y 217 pediatras, con el apoyo de 20 laboratorios.
De los 2579 aislamientos virales procedentes de la red centinela:
- 57,4 % correspondieron a virus A. De los subtipados: 84 % A(H1N1)pdm09 y 16 % A(H3N2).
- 42,4 % a virus B, casi todos de linaje Victoria.
 Cobertura vacunal
Cobertura vacunal
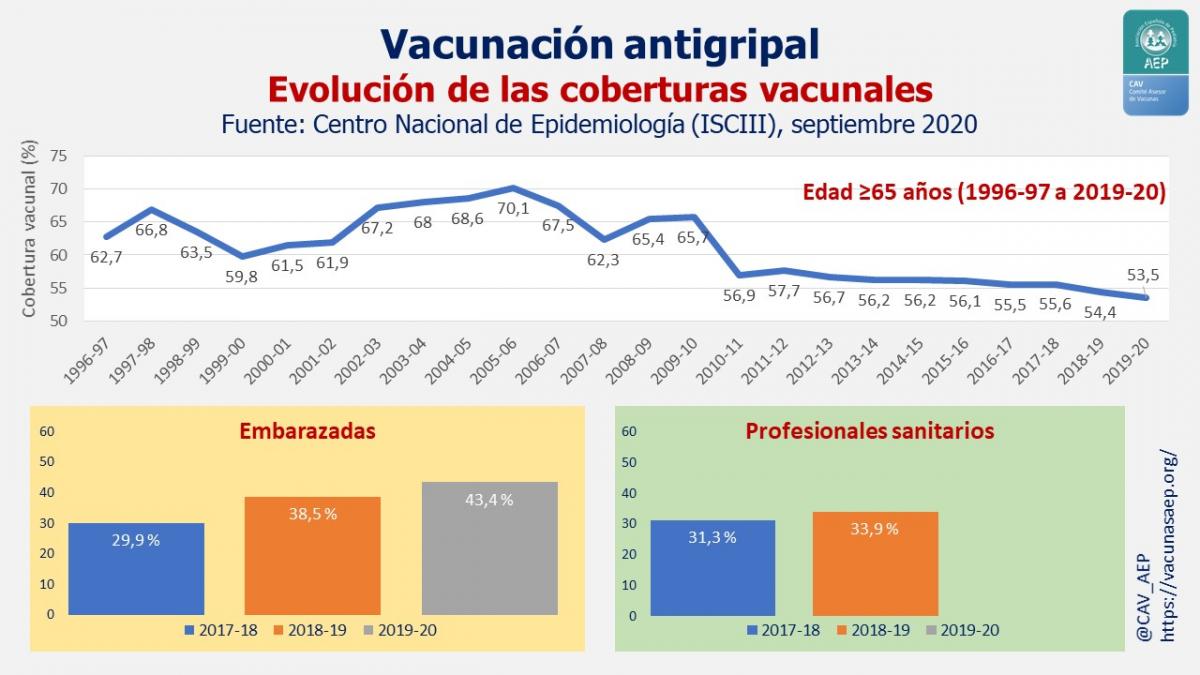
La evolución de las coberturas vacunales frente a la gripe (ver imagen de arriba y tabla·1 adjunta):
- Vacunación de las personas de 65 o más años de edad: caída de 9 puntos tras la temporada 2009-2010 [irrupción de la cepa pandémica A(H1N1)], seguida de una cierta estabilidad con tendencia a la baja desde entonces. En la temporada 2019-2020 la cobertura fue del 53,5·%, la más baja de los últimos 24 años.
- Respecto a la vacunación de las embarazadas y los profesionales sanitarios solo se conocen los datos de las dos últimas temporadas. En el caso de las gestantes se ha observado un incremento importante de la cobertura (casi 14 puntos porcentuales en dos años).
Impacto de la gripe estacional en España
Según los datos aportados por el CNE, la gripe ha tenido un impacto moderado en la temporada 2019-2020 (menor que en las dos temporadas anteriores) y habría ocasionado (ver imagen y tabla 2 adjuntas):
- 619.000 casos de gripe confirmadas en Atención Primaria.
- 27.700 hospitalizaciones con gripe confirmada (tasa acumulada de casos graves hospitalizados con gripe confirmada: 17,7 casos/100.000 hab.). El 47 % se concentraron en los de >64 años de edad, en el 89,7 % se trató de un virus A, y 9 de cada 10 de estos, A(H1N1).
- 1800 ingresos en unidades de cuidados intensivos con gripe confirmada.
- 3900 muertes atribuibles a la gripe.
| Tabla 1.- Cobertura vacunal frente a la gripe, temporadas 2017-18 a 2019-20 | |||
|---|---|---|---|
| Temporadas | 2017-18 | 2018-19 | 2019-20 |
| Más de 64 años | 55,6 % | 54,4 % | 53,5 % |
| Gestantes | 29,9 % | 38,5 % | 43,4 % |
| Profesionales sanitarios | 31,1 % | 35 % | |
| Fuente: Instituto de Salud Carlos III, infografías 2017-18 a 2019-20 y Ministerio de Sanidad, coberturas vacunales | |||
| Tabla 2.- Estimación de impacto de la gripe estacional en España, temporadas 2017-18 a 2019-20 | |||
|---|---|---|---|
| Temporadas | 2017-18 | 2018-19 | 2019-20 |
| Casos en AP | 700.000 | 490.000 | 619.000 |
| Hospitalizaciones | 52.000 | 35.300 | 27.700 |
| Ingresos UCI | 3000 | 2500 | 1800 |
| Muertes | 15.000 | 6300 | 3900 |
| Fuente: Instituto de Salud Carlos III, infografías 2017-18 a 2019-20 | |||
Impacto de la vacunación antigripal en España
Teniendo en cuenta una cobertura del 53,5·% en los mayores de 64 años en la temporada 2019-2020, la vacunación antigripal habría prevenido (ver imagen y tabla 3 adjuntas):
- 26 % de hospitalizaciones.
- 40 % de los ingresos en las unidades de cuidados intensivos.
- 37 % de las muertes atribuibles a la gripe.
| Tabla 3.- Impacto de la vacunación antigripal de >64 años en España, temporadas 2017-18 a 2019-20 | |||
|---|---|---|---|
| Temporadas | 2017-18 | 2018-19 | 2019-20 |
| Hospitalizaciones evitadas | 17 % | 11 % | 26 % |
| Ingresos UCI evitados | 40 % | 40 % | |
| Muertes evitadas | 39 % | 38 % | 37 % |
| Fuente: Instituto de Salud Carlos III, infografías 2017-18 a 2019-20 | |||
En cuanto a la vacunación de las gestantes (43,4 % en 2019-2020), un estudio referido al periodo 2017-2019, habría prevenido la hospitalización por gripe grave en lactantes menores de 6 meses de edad con una efectividad del 61 % (IC 95 %: 27-79 %) (Vaccine. 2020, 31 de julio, DOI: 10.1016/j.vaccine.2020.07.014).
Impacto de la pandemia de COVID-19 en la temporada gripal en el hemisferio sur
En el hemisfero sur la temporada gripal va desde el mes de febrero hasta el de septiembre, con el periodo de máxima incidencia entre mayo y julio. En este 2020, la temporada gripal ha coincidido con los primeros meses de la pandemia de COVID-19, declarada por la OMS el pasado 11 de marzo.
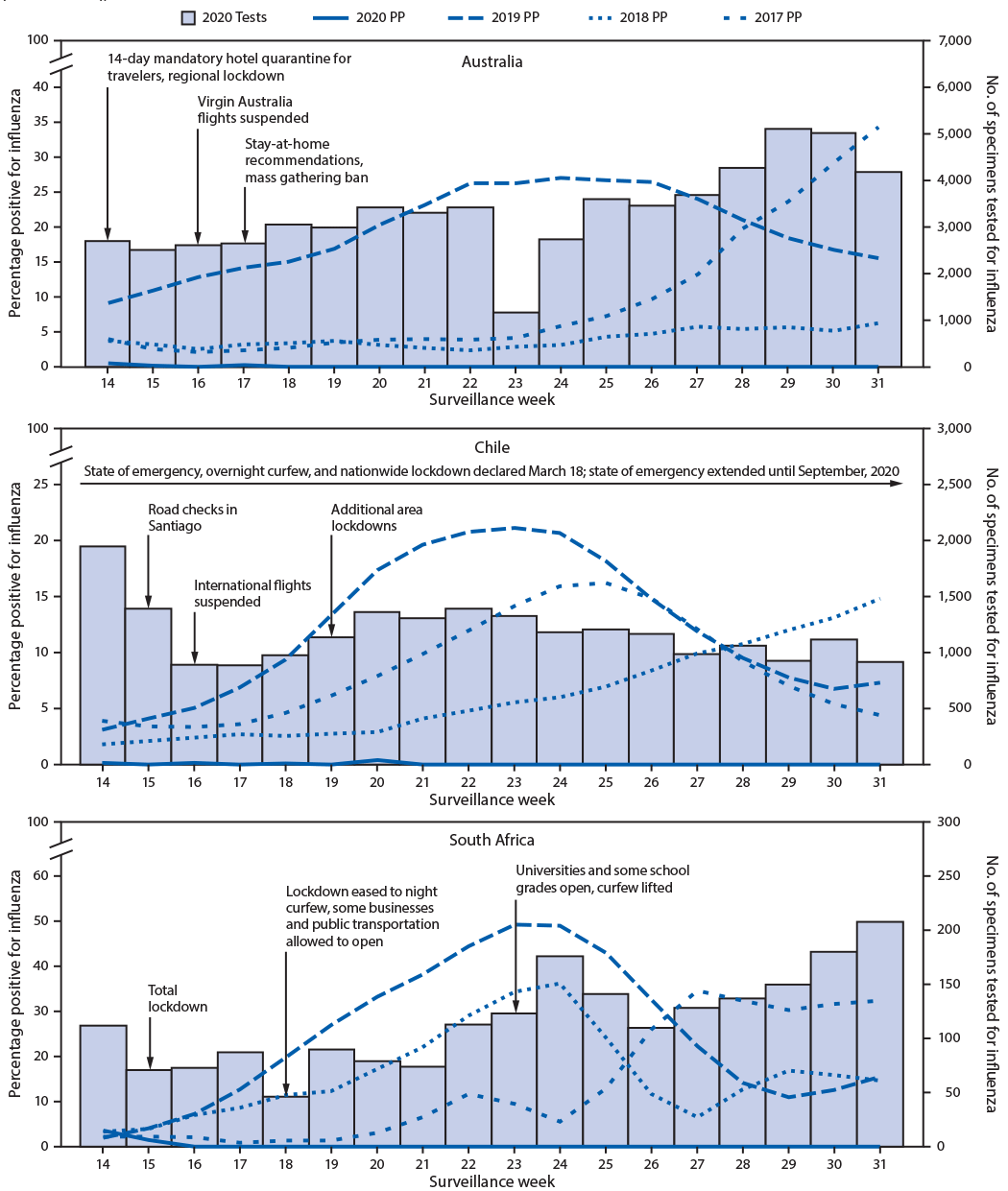
La coincidencia de la temporada gripal y las primeras fases de extensión de la pandemia ha tenido como consecuencia una reducción importante de la incidencia de gripe en varios países del hemisferio sur, como Australia, Chile y Sudáfrica (MMWR Morb Mortal Wkly Rep. 2020;69(37);1305-9).
Se estima que la elevada reducción observada (líneas de incidencia 2020 prácticamente en “cero”) podría obedecer a los efectos de las medidas higiénicas, el uso universal de las mascarillas faciales, el distanciamiento físico y la limitación de la movilidad.
¿Cuál será el impacto de la pandemia de COVID-19 en la temporada gripal 2020-2021 en España?
Es una incógnita pese a que lo observado en el hemisferio sur, que termina ahora su temporada gripal, llama a la calma. No obstante, tras la terrible experiencia vivida en los meses de marzo a mayo pasados, resulta imprescindible tomar todas las precauciones para reducir en lo posible el impacto acumulado de la COVID-19 y gripe, reforzando las medidas de higiene respiratoria y distanciamiento físico, además de la vacunación antigripal.
Más información:
- Temporada gripal 2020-2021: Recomendaciones del CAV-AEP de vacunación en niños y adolescentes. Vacunas antigripales de uso pediátrico disponibles. Composición de las vacunas antigripales.
- Temporada gripal 2019-2020: Instituto de Salud Carlos III. Sistema de Vigilancia de la Gripe en España. Informe de Vigilancia de la Gripe en España. Temporada 2019-2020. Estimación provisional de la efectividad vacunal. Fuentes de información y definiciones, septiembre de 2019. Guía de procedimientos, cotubre de 2019.
- Temporada gripal 2018-2019: Balance global. Infografía resumen.
- Temporada gripal 2017-2018: infografía resumen.
- ECDC, 6 de agosto de 2020. Seasonal influenza – Annual Epidemiological Report for 2019-2020.
- OMS, vigilancia y monitorización de la gripe.
- Otras noticias anteriores sobre la gripe y sus vacunas en esta web.
- La vacunación antigripal en el Manual de vacunas en línea de la AEP.
Es muy importante conocer cuales son las falsas contraindicaciones de las vacunas, para evitar oportunidades perdidas; pero no solamente conllevan retrasos innecesarios para la adecuada protección, sino que además favorecen la propagación en la sociedad de creencias erróneas con relación a las situaciones en las que se puede o no se puede vacunar.
Existe una larga lista de circunstancias consideradas contraindicaciones sin serlo. Entre las más frecuentes destacan las mostradas en la tabla 1:
Tabla 1. Falsas contraindicaciones y precauciones frente a las vacunas.
| Vacuna | Circunstancias habitualmente percibidas de forma errónea como contraindicación o precaución |
| En general, para todas las vacunas, incluyendo DTPa, Td, Tdpa, SRP, Hib, hepatitis A, hepatitis B, varicela, rotavirus, VNC, antigripal inactivada, VNP23, Polio, Men·ACWY y VPH |
– Enfermedad aguda leve, con o sin fiebre – Reacción local leve o moderada (es decir, hinchazón, enrojecimiento, dolor) – Fiebre baja o moderada después de la dosis anterior – Ausencia de examen físico previo, en persona con apariencia sana – Terapia antimicrobiana actual (a) – Fase de enfermedad convaleciente – Prematuridad – Exposición reciente a una enfermedad infecciosa – Historia de alergia a la penicilina, otras alergias no causadas por la vacuna o a componentes no incluidos en la vacuna, familiares con alergias o estar recibiendo inmunoterapia con extractos de alérgenos, solo se tendrá la precaución de aplicarlos en miembros distintos – Historia de síndrome de Guillain-Barré (b) – Historia familiar de efectos adversos tras las vacunas – Antecedentes de convulsiones febriles o epilepsia estable – Haber padecido la enfermedad para la que se vacuna, ya que en todo caso incrementará la inmunidad frente a ella. (p. ej., tosferina) – Tratamiento con corticoides tópicos o inhalados o con dosis fisiológicas de reemplazo con corticoides sistémicos – Antecedentes de asma, eccema o atopia – Antecedentes de síndrome pertusoide, sarampión, rubeola, parotiditis, varicela, herpes zóster o enfermedad meningocócica – Patologías diversas: parálisis cerebral, síndrome de Down, ictericia neonatal, bajo peso al nacer, cirugía reciente (si cirugía mayor, demorar las vacunas 2 semanas tras la intervención, valorando siempre el beneficio/riesgo) o inminente (salvo vacunas de virus atenuados en las 4 semanas previas a un trasplante de órgano sólido) – Lactancia materna (tanto en lo que se refiere a la madre como al lactante), salvo en el caso de la vacunación materna contra la fiebre amarilla (ver capítulo 24) y precaución en el caso de la vacunación materna frente a la varicela por si apareciera reacción exantemática local o general a la vacuna, en cuyo caso, por precaución, la madre no contactará con el lactante – Contacto domiciliario con personas inmunodeficientes (con la excepción de la vacuna antipoliomielítica oral) – Contacto con enfermedad infecciosa – Registros vacunales previos no conocidos – Hospitalización: el niño hospitalizado puede recibir las vacunas que precise en las unidades neonatales hospitalarias, incluida la vacuna frente al rotavirus, según las recomendaciones actuales |
| DTPa | – Historia de fiebre de ≥40,5 °C durante <48 horas después de la vacunación con una dosis previa de DTP/DTPa/Tdpa – Colapso o estado parecido a un shock (episodio de hipotonía-hiporrespuesta) dentro de las 48 horas tras recibir una dosis de DTP/DTPa/Tdpa – Convulsión ≤3 días después de recibir una dosis de DTP/DTPa/Tdpa – Llanto persistente e inconsolable que dura ≥3 horas dentro de las 48 horas después de recibir una dosis de DTP/DTPa/Tdpa – Antecedentes familiares de convulsiones – Antecedentes familiares de síndrome de muerte súbita del lactante – Antecedentes familiares de un evento adverso después de la administración de DTP/DTPa/Tdpa – Condiciones neurológicas estables (p. ej., parálisis cerebral, epilepsia bien controlada o retraso en el desarrollo neurológico) |
| Gripe atenuada (intranasal) |
– Profesionales sanitarios que atienden a pacientes con enfermedades crónicas o inmunodeprimidos (una excepción son los que atienden a pacientes con inmunodepresión grave que requieren atención en un entorno protegido) – Amamantamiento – Contactos de personas con enfermedades crónicas o inmunodeprimidos (una excepción son los contactos de pacientes gravemente inmunodeprimidos que requieren atención en un entorno protegido) |
| Gripe inactivada (inyectable) |
– Alergia no grave (p. ej., por contacto) al látex o al tiomersal – Alergia anafiláctica al huevo – Administración concurrente de warfarina o aminofilina |
| Hepatitis B | – Embarazo – Enfermedad autoinmune (p. ej., lupus eritematoso sistémico o artritis reumatoide) – Inmunosupresión |
| Neumococo polisacarídica (VNP23) | – Historia de enfermedad neumocócica invasora o neumonía |
| Polio inactivada | – Administración previa de ≥1 dosis de vacuna atenuada oral frente a la polio |
| Rotavirus | – Prematuridad – Contactos domésticos inmunodeprimidos – Contactos embarazadas en el hogar |
| SRP (triple vírica) (c) (d) |
– Prueba cutánea de la tuberculina positiva – Prueba simultánea de tuberculina en la piel o ensayo de liberación de interferón gamma (IGRA) (e) – Amamantamiento – Embarazo de la madre del receptor u otro contacto cercano o familiar – Mujer en edad fértil – Contacto familiar o familiar inmunodeficiente – Infección por VIH asintomática o levemente sintomática – Alergia al huevo de cualquier tipo, incluida la anafiláctica |
| Tdpa | – Historia de fiebre de ≥40,5 °C durante <48 horas después de la vacunación con una dosis previa de DTP/DTPa/Tdpa – Historia de colapso o estado de shock (es decir, episodio de hipotonía hiporrespuesta) dentro de las 48 horas posteriores a la administración de una dosis previa de DTP/DTPa/Tdpa – Antecedentes de convulsión <3 días después de recibir una dosis previa de DTP/DTPa/Tdpa – Antecedentes de llanto persistente e inconsolable que dura más de 3 horas, dentro de las 48 horas después de recibir una dosis previa de DTP/DTPa/Tdpa – Historial de hinchazón extensa de las extremidades después de DTP/DTPa/Tdpa/Td que no se trate de una reacción de tipo Arthus – Historia de trastorno neurológico estable – Historia de neuritis braquial – Alergia al látex no anafiláctica – Amamantamiento – Inmunosupresión |
| Varicela | – Embarazo de la madre del receptor u otro contacto cercano o familiar – Contacto familiar o familiar inmunodeficiente (f) – Infección por VIH asintomática o levemente sintomática – Inmunodeficiencia humoral (p. ej., agammaglobulinemia) |
| Virus Papiloma Humano | – Prueba previa de Papanicolaou alterada – Infección conocida por VPH – Amamantamiento – Historia de verrugas genitales |
Abreviaturas: DTP = toxoide diftérico, toxoide tetánico y tosferina de células enteras; DTPa = toxoides tetánico y diftérico y tosferina acelular de carga estándar; Hib = Haemophilus influenzae tipo b; Men·ACWY = vacuna tetravalente conjugada meningocócica; SRP = sarampión, rubeola y paperas; Td = toxoides tetánico y diftérico de carga reducida; Tdpa = toxoide tetánico, toxoide diftérico reducido y tosferina acelular de carga reducida; VIH = virus de la inmunodeficiencia humana; VNC = vacuna antineumocócica conjugada; VNP23 = vacuna polisacárida neumocócica de 23 serotipos; VPH = virus del papiloma humano; VPI = poliovirus inactivado.
(a) Los antibióticos podrían interferir con la vacuna tifoidea oral Ty21a y ciertos medicamentos antivirales pueden interferir con las vacunas que contienen el componente varicela.
(b) Una excepción es el síndrome de Guillain-Barré dentro de las 6 semanas siguientes a una dosis de vacuna frente a la gripe o de vacuna que contiene toxoide tetánico, que son precauciones para las vacunas frente a la gripe y las vacunas que contienen toxoide tetánico, respectivamente.
(c) Las vacunas TV y varicela se pueden administrar el mismo día. Si no se administran el mismo día, estas vacunas deben separarse por, al menos, 28 días.
(d) Los niños infectados por el VIH deben recibir inmunoglobulina después de la exposición al sarampión. Los niños infectados por el VIH pueden recibir la vacuna contra la varicela y el sarampión si el recuento de linfocitos T CD4+ es >15 %.
(e) La vacunación contra el sarampión podría suprimir temporalmente la reactividad de la tuberculina. La vacuna que contiene el sarampión se puede administrar el mismo día que la prueba de la tuberculina o IGRA. Si las pruebas no pueden realizarse hasta después del día de la vacunación TV, la prueba debe posponerse durante, al menos, 4 semanas después de la vacunación. Si existe una necesidad urgente de realizar una prueba cutánea o IGRA, hágalo con el entendimiento de que la vacuna puede reducir la reactividad.
(f) Si un vacunado experimenta una erupción supuestamente relacionada con la vacuna 7-25 días después de la vacunación, la persona debe evitar el contacto con personas inmunocomprometidas durante la erupción.
Fuente: Modificado de Advisory Committee on Immunization Practices (ACIP). Contraindications and Precautions. Vaccine Recommendations and Guidelines of the ACIP: General Best Practice Guidelines for Immunization (2018).
BIBLIOGRAFÍA
- Centers for Disease Control and Prevention. Epidemiology and Prevention of Vaccine-Preventable Diseases. Atkinson W, Wolfe S, Hamborsky J (eds.). Chapter 2 General Recommendations on Immunization. 13th ed. Washington DC: Public Health Foundation, 2015. Disponible en: http://www.cdc.gov/vaccines/pubs/pinkbook/genrec.html
- Centers for Disease Control and Prevention. Chart of Contraindications and Precautions to Commonly Used Vaccines. November 2020. https://www.cdc.gov/vaccines/hcp/acip-recs/general-recs/contraindication…
- Comité Asesor de Vacunas (CAV-AEP). Seguridad de las vacunas. Contraindicaciones y precauciones. Manual de vacunas en línea de la AEP [Internet]. Madrid: AEP; ene/2019. [consultado el 01/ene/2021]. Disponible en: http://vacunasaep.org/documentos/manual/cap-3
Un aspecto muy importante vinculado a la seguridad de las vacunas es conocer las precauciones y contraindicaciones de cada vacuna con la finalidad de evitar situaciones que puedan poner en riesgo al paciente.
Las precauciones y contraindicaciones, definidas en la ficha técnica de cada vacuna, pueden cambiar con el tiempo, por lo que deben revisarse las fichas actualizadas.
El profesional que administra vacunas es responsable de conocer tanto las contraindicaciones como las precauciones vigentes en el país en el que ejerce.
Antes de vacunar se comprobará si el paciente tiene contraindicaciones temporales o permanentes para ser vacunado.
Contraindicaciones
Es una condición del individuo que aumenta de forma importante el riesgo de padecer un efecto adverso grave si se le administra una vacuna concreta.
Solo dos situaciones se consideran contraindicaciones permanentes y nunca podrá administrarse la vacuna.
La mayoría de las contraindicaciones son temporales y una vez pasada esa situación el paciente podrá ser vacunado.
CONTRAINDICACIONES PERMANENTES
- Una reacción alérgica anafiláctica a una dosis previa de una vacuna o a algún componente de la misma es una contraindicación permanente para volver a administrar dicha vacuna o cualquier otra vacuna que contenga dicho componente.
- La presencia de una encefalopatía de etiología desconocida aparecida en los 7 días siguientes a la administración de una vacuna con componente frente a la tosferina contraindica la administración de dosis posteriores de vacunas que contengan dicho componente. La vacuna Td también está autorizada en menores de 7 años cuando haya contraindicación para la vacuna de la tosferina.
CONTRAINDICACIONES TEMPORALES
El embarazo y la inmunodepresión o inmunosupresión son los dos ejemplos más comunes de contraindicación temporal, únicamente para las vacunas víricas o bacterianas atenuadas.
Las contraindicaciones temporales permiten la administración de una vacuna una vez resueltas.
- Embarazo: el embarazo es una situación que contraindica de forma temporal la administración de cualquier vacuna atenuada ya sea vírica o bacteriana. Los registros de mujeres vacunadas inadvertidamente durante el embarazo con triple vírica o varicela demuestran que no se han producido casos de síndrome de rubeola congénita ni de varicela congénita, por lo que la administración inadvertida de estas vacunas durante el embarazo no constituye un motivo de interrupción del embarazo; además el riesgo en todo caso es mucho menor que el de la infección natural durante el embarazo. Por otro lado las vacunas inactivadas se pueden (y algunas se deben) administrar en el embarazo; como ejemplo la vacuna de la gripe en cualquier trimestre del embarazo y la vacuna de la tosferina (Tdpa) entre la 27 y 36 semanas de gestación.
- Inmunodepresión. La inmunodepresión o el tratamiento inmunosupresor contraindican, con algunas excepciones, las vacunas atenuadas; los niños con niveles de linfocitos CD4+ superiores al 15 % pueden recibir las vacunas triple vírica y la de la varicela. Esta inmunodepresión puede condicionar una respuesta inadecuada de las vacunas inactivadas, que se podrán administrar, aunque posteriormente es posible que precisen dosis adicionales. En nuestro país los niños sanos que conviven con personas inmunodeprimidas pueden y deben recibir todas las vacunas de calendario que les correspondan por su edad, incluidas las de virus vivos como triple vírica (sarampión, rubeola o parotiditis), varicela y rotavirus, asimismo deben vacunarse anualmente frente a la gripe si tienen, al menos, 6 meses de edad.
- Cualquier enfermedad moderada o grave (crisis asmática, cardiopatía descompensada, diarrea aguda…), con o sin fiebre, es una contraindicación temporal para la administración de las vacunas, salvo situación de riesgo epidémico muy elevado. Una vez desparecida la situación podrán recibir vacunas.
- La edad de administración puede considerarse una contraindicación. La vacuna triple vírica no se aconseja administrarla antes de los 12 meses de vida porque puede interferir con los anticuerpos maternos y no producir una respuesta inmunológica completa, aunque en situaciones epidémicas se puede administrar a partir de los 6 meses de edad, aunque posteriormente deberá recibir dos dosis a partir de que cumpla los 12 meses de edad. Igualmente, la vacuna frente a la hepatitis A se administra a partir de los 12 meses de edad, la antigripal a partir de los 6 meses de edad y los componentes de carga antigénica estándar de difteria y tosferina (D y P) solo se pueden aplicar hasta los 7 años de eda
Precauciones o limitaciones para la vacunación
Son situaciones en las que la administración de una vacuna condiciona un mayor riesgo de presentar un efecto adverso o bien que la respuesta inmunitaria a la vacuna pueda ser insuficiente y no permita obtener una adecuada protección.
Una precaución indica que debe valorarse el cociente riesgo/beneficio antes de decidir la administración de la vacuna en cuestión. En determinadas circunstancias en las que el beneficio es superior al riesgo (p. e. situación de epidemia) la vacuna puede administrarse.
Algunas situaciones consideradas precauciones son:
- Trastorno neurológico progresivo, incluidos espasmos infantiles, epilepsia no controlada y encefalopatía progresiva. En estos casos se recomienda retrasar la vacunación de la tosferina hasta la estabilización del proceso.
- Historia de síndrome de Guillain-Barré en las 6 semanas posteriores a la administración de una vacuna. En este caso deberá valorarse con precaución la conveniencia o no de administrar una dosis posterior de dicha vacuna.
- Pacientes con enfermedades crónicas y/o inmunodepresión: la respuesta a la vacunación puede ser subóptima en algunos de estos pacientes, por lo que las vacunas deben administrarse atendiendo a este hecho. Se ha comentado previamente que en caso de inmunodepresión las vacunas atenuadas están contraindicadas en la mayoría de las situaciones.
- La administración de productos biológicos (inmunoglobulinas o sangre) antes de la administración de la vacuna triple vírica o la de la varicela (ver capítulo 43).
- Una excepción a la anafilaxia como contraindicación son los niños con alergia anafiláctica al huevo, ya que pueden recibir la vacuna triple vírica en el centro de salud, porque prácticamente no tiene proteínas de huevo, esperando posteriormente 15-30 minutos en la sala de espera como con todas las vacunas y actualmente, también, pueden recibir vacunas inactivadas frente a la gripe en el centro de salud.
FALSAS CONTRAINDICACIONES
Es muy importante conocer cuales son las falsas contraindicaciones de las vacunas, para evitar oportunidades perdidas; pero no solamente conllevan retrasos innecesarios para la adecuada protección, sino que además favorecen la propagación en la sociedad de creencias erróneas con relación a las situaciones en las que se puede o no se puede vacunar.
Existe una larga lista de circunstancias consideradas contraindicaciones sin serlo. Entre las más frecuentes destacan las mostradas en la tabla 1:
Tabla 1. Falsas contraindicaciones y precauciones frente a las vacunas.
| Vacuna | Circunstancias habitualmente percibidas de forma errónea como contraindicación o precaución |
| En general, para todas las vacunas, incluyendo DTPa, Td, Tdpa, SRP, Hib, hepatitis A, hepatitis B, varicela, rotavirus, VNC, antigripal inactivada, VNP23, Polio, Men·ACWY y VPH |
– Enfermedad aguda leve, con o sin fiebre – Reacción local leve o moderada (es decir, hinchazón, enrojecimiento, dolor) – Fiebre baja o moderada después de la dosis anterior – Ausencia de examen físico previo, en persona con apariencia sana – Terapia antimicrobiana actual (a) – Fase de enfermedad convaleciente – Prematuridad – Exposición reciente a una enfermedad infecciosa – Historia de alergia a la penicilina, otras alergias no causadas por la vacuna o a componentes no incluidos en la vacuna, familiares con alergias o estar recibiendo inmunoterapia con extractos de alérgenos, solo se tendrá la precaución de aplicarlos en miembros distintos – Historia de síndrome de Guillain-Barré (b) – Historia familiar de efectos adversos tras las vacunas – Antecedentes de convulsiones febriles o epilepsia estable – Haber padecido la enfermedad para la que se vacuna, ya que en todo caso incrementará la inmunidad frente a ella. (p. ej., tosferina) – Tratamiento con corticoides tópicos o inhalados o con dosis fisiológicas de reemplazo con corticoides sistémicos – Antecedentes de asma, eccema o atopia – Antecedentes de síndrome pertusoide, sarampión, rubeola, parotiditis, varicela, herpes zóster o enfermedad meningocócica – Patologías diversas: parálisis cerebral, síndrome de Down, ictericia neonatal, bajo peso al nacer, cirugía reciente (si cirugía mayor, demorar las vacunas 2 semanas tras la intervención, valorando siempre el beneficio/riesgo) o inminente (salvo vacunas de virus atenuados en las 4 semanas previas a un trasplante de órgano sólido) – Lactancia materna (tanto en lo que se refiere a la madre como al lactante), salvo en el caso de la vacunación materna contra la fiebre amarilla (ver capítulo 24) y precaución en el caso de la vacunación materna frente a la varicela por si apareciera reacción exantemática local o general a la vacuna, en cuyo caso, por precaución, la madre no contactará con el lactante – Contacto domiciliario con personas inmunodeficientes (con la excepción de la vacuna antipoliomielítica oral) – Contacto con enfermedad infecciosa – Registros vacunales previos no conocidos – Hospitalización: el niño hospitalizado puede recibir las vacunas que precise en las unidades neonatales hospitalarias, incluida la vacuna frente al rotavirus, según las recomendaciones actuales |
| DTPa | – Historia de fiebre de ≥40,5 °C durante <48 horas después de la vacunación con una dosis previa de DTP/DTPa/Tdpa – Colapso o estado parecido a un shock (episodio de hipotonía-hiporrespuesta) dentro de las 48 horas tras recibir una dosis de DTP/DTPa/Tdpa – Convulsión ≤3 días después de recibir una dosis de DTP/DTPa/Tdpa – Llanto persistente e inconsolable que dura ≥3 horas dentro de las 48 horas después de recibir una dosis de DTP/DTPa/Tdpa – Antecedentes familiares de convulsiones – Antecedentes familiares de síndrome de muerte súbita del lactante – Antecedentes familiares de un evento adverso después de la administración de DTP/DTPa/Tdpa – Condiciones neurológicas estables (p. ej., parálisis cerebral, epilepsia bien controlada o retraso en el desarrollo neurológico) |
| Gripe atenuada (intranasal) |
– Profesionales sanitarios que atienden a pacientes con enfermedades crónicas o inmunodeprimidos (una excepción son los que atienden a pacientes con inmunodepresión grave que requieren atención en un entorno protegido) – Amamantamiento – Contactos de personas con enfermedades crónicas o inmunodeprimidos (una excepción son los contactos de pacientes gravemente inmunodeprimidos que requieren atención en un entorno protegido) |
| Gripe inactivada (inyectable) |
– Alergia no grave (p. ej., por contacto) al látex o al tiomersal – Alergia anafiláctica al huevo – Administración concurrente de warfarina o aminofilina |
| Hepatitis B | – Embarazo – Enfermedad autoinmune (p. ej., lupus eritematoso sistémico o artritis reumatoide) – Inmunosupresión |
| Neumococo polisacarídica (VNP23) | – Historia de enfermedad neumocócica invasora o neumonía |
| Polio inactivada | – Administración previa de ≥1 dosis de vacuna atenuada oral frente a la polio |
| Rotavirus | – Prematuridad – Contactos domésticos inmunodeprimidos – Contactos embarazadas en el hogar |
| SRP (triple vírica) (c) (d) |
– Prueba cutánea de la tuberculina positiva – Prueba simultánea de tuberculina en la piel o ensayo de liberación de interferón gamma (IGRA) (e) – Amamantamiento – Embarazo de la madre del receptor u otro contacto cercano o familiar – Mujer en edad fértil – Contacto familiar o familiar inmunodeficiente – Infección por VIH asintomática o levemente sintomática – Alergia al huevo de cualquier tipo, incluida la anafiláctica |
| Tdpa | – Historia de fiebre de ≥40,5 °C durante <48 horas después de la vacunación con una dosis previa de DTP/DTPa/Tdpa – Historia de colapso o estado de shock (es decir, episodio de hipotonía hiporrespuesta) dentro de las 48 horas posteriores a la administración de una dosis previa de DTP/DTPa/Tdpa – Antecedentes de convulsión <3 días después de recibir una dosis previa de DTP/DTPa/Tdpa – Antecedentes de llanto persistente e inconsolable que dura más de 3 horas, dentro de las 48 horas después de recibir una dosis previa de DTP/DTPa/Tdpa – Historial de hinchazón extensa de las extremidades después de DTP/DTPa/Tdpa/Td que no se trate de una reacción de tipo Arthus – Historia de trastorno neurológico estable – Historia de neuritis braquial – Alergia al látex no anafiláctica – Amamantamiento – Inmunosupresión |
| Varicela | – Embarazo de la madre del receptor u otro contacto cercano o familiar – Contacto familiar o familiar inmunodeficiente (f) – Infección por VIH asintomática o levemente sintomática – Inmunodeficiencia humoral (p. ej., agammaglobulinemia) |
| Virus Papiloma Humano | – Prueba previa de Papanicolaou alterada – Infección conocida por VPH – Amamantamiento – Historia de verrugas genitales |
Abreviaturas: DTP = toxoide diftérico, toxoide tetánico y tosferina de células enteras; DTPa = toxoides tetánico y diftérico y tosferina acelular de carga estándar; Hib = Haemophilus influenzae tipo b; Men·ACWY = vacuna tetravalente conjugada meningocócica; SRP = sarampión, rubeola y paperas; Td = toxoides tetánico y diftérico de carga reducida; Tdpa = toxoide tetánico, toxoide diftérico reducido y tosferina acelular de carga reducida; VIH = virus de la inmunodeficiencia humana; VNC = vacuna antineumocócica conjugada; VNP23 = vacuna polisacárida neumocócica de 23 serotipos; VPH = virus del papiloma humano; VPI = poliovirus inactivado.
(a) Los antibióticos podrían interferir con la vacuna tifoidea oral Ty21a y ciertos medicamentos antivirales pueden interferir con las vacunas que contienen el componente varicela.
(b) Una excepción es el síndrome de Guillain-Barré dentro de las 6 semanas siguientes a una dosis de vacuna frente a la gripe o de vacuna que contiene toxoide tetánico, que son precauciones para las vacunas frente a la gripe y las vacunas que contienen toxoide tetánico, respectivamente.
(c) Las vacunas TV y varicela se pueden administrar el mismo día. Si no se administran el mismo día, estas vacunas deben separarse por, al menos, 28 días.
(d) Los niños infectados por el VIH deben recibir inmunoglobulina después de la exposición al sarampión. Los niños infectados por el VIH pueden recibir la vacuna contra la varicela y el sarampión si el recuento de linfocitos T CD4+ es >15 %.
(e) La vacunación contra el sarampión podría suprimir temporalmente la reactividad de la tuberculina. La vacuna que contiene el sarampión se puede administrar el mismo día que la prueba de la tuberculina o IGRA. Si las pruebas no pueden realizarse hasta después del día de la vacunación TV, la prueba debe posponerse durante, al menos, 4 semanas después de la vacunación. Si existe una necesidad urgente de realizar una prueba cutánea o IGRA, hágalo con el entendimiento de que la vacuna puede reducir la reactividad.
(f) Si un vacunado experimenta una erupción supuestamente relacionada con la vacuna 7-25 días después de la vacunación, la persona debe evitar el contacto con personas inmunocomprometidas durante la erupción.
Fuente: Modificado de Advisory Committee on Immunization Practices (ACIP). Contraindications and Precautions. Vaccine Recommendations and Guidelines of the ACIP: General Best Practice Guidelines for Immunization (2018).
BIBLIOGRAFÍA
- Centers for Disease Control and Prevention. Epidemiology and Prevention of Vaccine-Preventable Diseases. Atkinson W, Wolfe S, Hamborsky J (eds.). Chapter 2 General Recommendations on Immunization. 13th ed. Washington DC: Public Health Foundation, 2015. Disponible en: http://www.cdc.gov/vaccines/pubs/pinkbook/genrec.html
- Centers for Disease Control and Prevention. Chart of Contraindications and Precautions to Commonly Used Vaccines. November 2020. https://www.cdc.gov/vaccines/hcp/acip-recs/general-recs/contraindication…
- Comité Asesor de Vacunas (CAV-AEP). Seguridad de las vacunas. Contraindicaciones y precauciones. Manual de vacunas en línea de la AEP [Internet]. Madrid: AEP; ene/2019. [consultado el 01/ene/2021]. Disponible en: http://vacunasaep.org/documentos/manual/cap-3